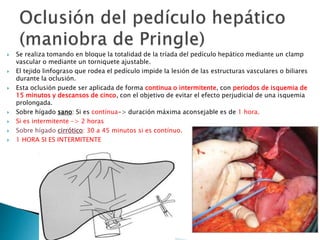
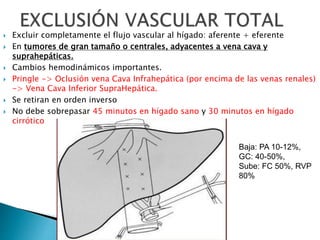
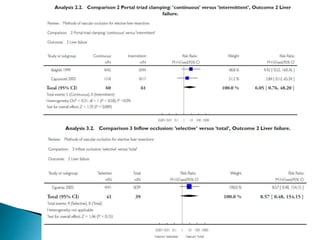
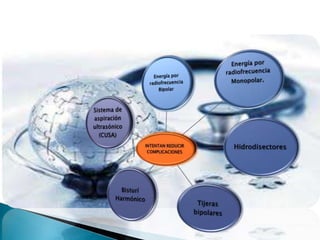
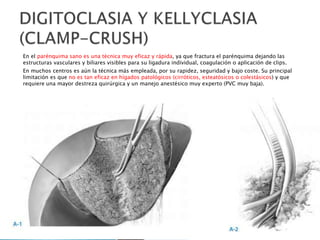
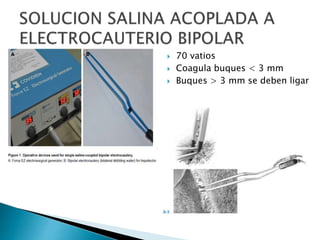
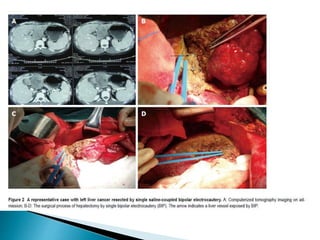
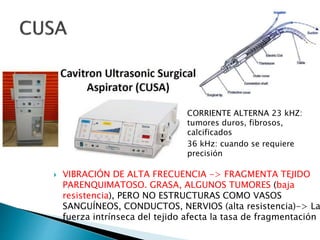
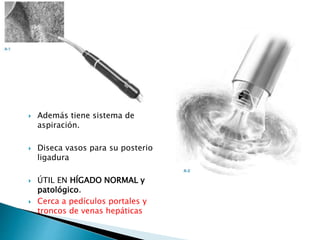
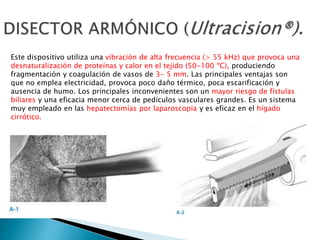
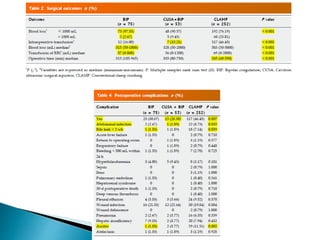
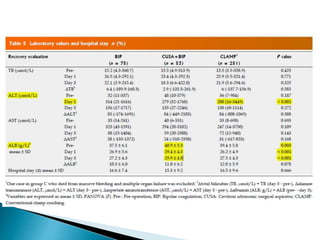
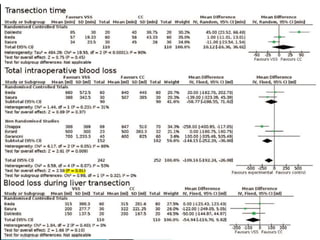
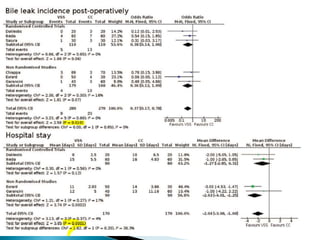
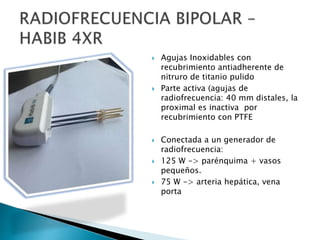
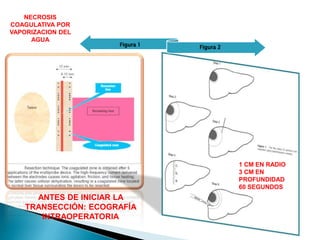
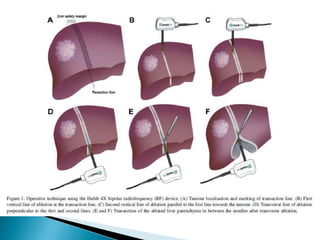
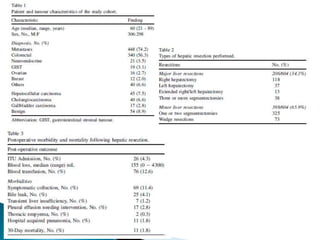
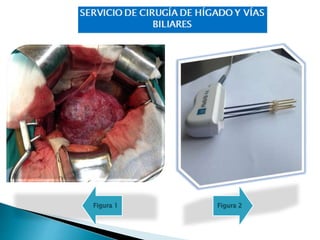
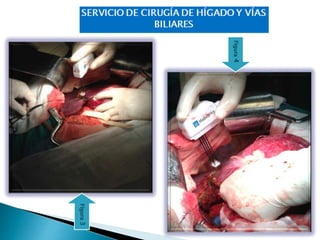
La cirugía hepática ha mejorado con técnicas como la anestesia hipotensiva y el clampaje del pedículo hepático para controlar complicaciones como la hemorragia, aunque aumenta la morbilidad en hígados enfermos. Métodos como laoclusión vascular y dispositivos como el bisturí eléctrico monopolar y sistemas de coagulación por radiofrecuencia han demostrado eficacia en la resección hepática, aunque presentan limitaciones dependiendo del estado del hígado. A pesar de las innovaciones, la elección de la técnica depende de la experiencia del cirujano y la condición del tejido hepático.