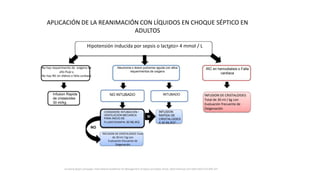
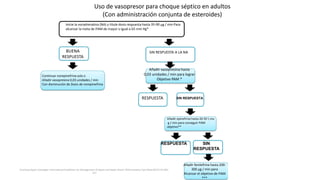
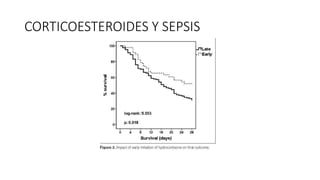
Este documento resume las principales pautas para el manejo de la sepsis y el choque séptico según la campaña Surviving Sepsis Campaign de 2016. Incluye recomendaciones sobre diagnóstico temprano, reanimación inicial con fluidos, antibioticoterapia dentro de la primera hora, control del estado hemodinámico y lactato, así como el uso de corticoides y hemocomponentes.