Mapa Menta del Química
•
1 recomendación•88 vistas
Mapa Mental de Química
Denunciar
Compartir
Denunciar
Compartir
Descargar para leer sin conexión
Recomendados
Más contenido relacionado
La actualidad más candente
La actualidad más candente (20)
Similar a Mapa Menta del Química
Similar a Mapa Menta del Química (20)
Último
Último (20)
PROBLEMAS DE GENÉTICA CON ÁRBOLES GENEALÓGICOS.pdf

PROBLEMAS DE GENÉTICA CON ÁRBOLES GENEALÓGICOS.pdf
Módulo No. 1 Salud mental y escucha activa FINAL 25ABR2024 técnicos.pptx

Módulo No. 1 Salud mental y escucha activa FINAL 25ABR2024 técnicos.pptx
Evaluación de los Factores Internos de la Organización

Evaluación de los Factores Internos de la Organización
ACERTIJO LA RUTA DE LAS ADIVINANZAS OLÍMPICAS. Por JAVIER SOLIS NOYOLA

ACERTIJO LA RUTA DE LAS ADIVINANZAS OLÍMPICAS. Por JAVIER SOLIS NOYOLA
Presentación Pedagoía medieval para exposición en clases

Presentación Pedagoía medieval para exposición en clases
Descripción anatómica de los músculos de la cabeza de equino y bovino (6).pdf

Descripción anatómica de los músculos de la cabeza de equino y bovino (6).pdf
ensayo literario rios profundos jose maria ARGUEDAS

ensayo literario rios profundos jose maria ARGUEDAS
PLAN DE TRABAJO CONCURSO NACIONAL CREA Y EMPRENDE.docx

PLAN DE TRABAJO CONCURSO NACIONAL CREA Y EMPRENDE.docx
Mapa Menta del Química
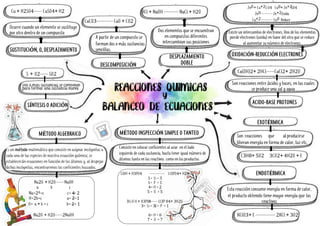
- 1. . SÍNTESIS O ADICIÓN Dos o más sustancias se combinan para formar una sustancia nueva S + O2----- SO2 DESCOMPOSICIÓN A partir de un compuesto se forman dos o más sustancias sencillas. CaCO3---------- CaO + CO2 SUSTITUCIÓN, O, DESPLAZAMIENTO Ocurre cuando un elemento se sustituye por otro dentro de un compuesto Cu + H2SO4----- CuSO4+ H2 Dos elementos que se encuentran en compuestos diferentes intercambian sus posiciones HCl + NaOH --------- NaCl + H2O ACIDO-BASE PROTONES Son reacciones entre ácidos y bases, en las cuales se produce una sal y agua Ca(OH)2+ 2HCl-----CaCl2+ 2H2O OXIDACIÓN-REDUCCIÓN ELECTRONES Existe un intercambio de electrones. Uno de los elementos pierde electrones (oxida) en favor del otro que se reduce al aumentar su número de electrones. Zn0+ Cu+2S O4 Cu0+ Zn+2SO4 Zn0--------- Zn+2Oxida Cu+2--------- Cu0 Reduce EXOTÉRMICA Son reacciones que alproducirse liberan energía en forma de calor, luz etc. C3H8+ 5O2 3CO2+ 4H2O + E KClO3+ E ------------ 2KCl + 3O2 Esta reacción consume energía en forma de calor, el producto obtenido tiene mayor energía que los reactivos ENDOTÉRMICA MÉTODO INSPECCIÓN SIMPLE O TANTEO Consiste en colocar coeficientes al azar en el lado izquierdo de cada sustancia, hasta tener igual número de átomos tanto en los reactivos como en los productos LIOH + H3PO4 ------------ LI3PO4+ H20 1= Li = 3 1= P = 1 4= H = 2 5 = O = 5 3Li O H + H3P04----- LI3P 04+ 3H2O 3= Li = 31= P = 1 6= H = 6 7 = O = 7 MÉTODO ALGEBRAICO Es un método matemático que consiste en asignar incógnitas a cada una de las especies de nuestra ecuación química; se establecerán ecuaciones en función de los átomos y, al despejar dichas incógnitas, encontraremos los coeficientes buscados. Na2O + H2O------NaOH a b c Na=2ª=c c= 4= 2 H=2b=c a= 2=1 O= a + b = c b= 2= 1 Na2O + H2O-----2NaOH DESPLAZAMIENTO DOBLE c c c c c c c c