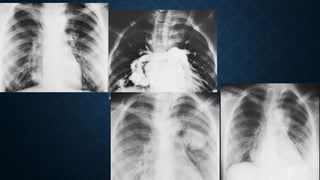
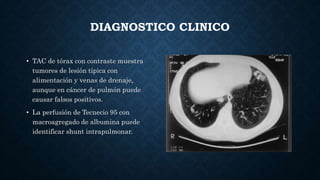
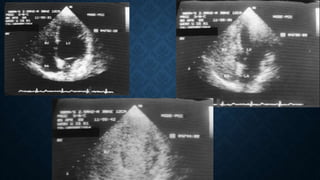
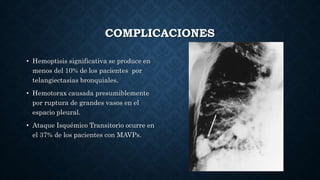
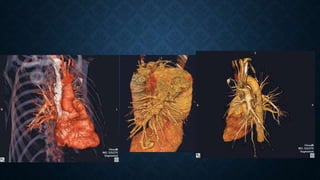
Este documento describe la historia, fisiopatología, genética, presentación clínica, diagnóstico y complicaciones de las malformaciones arteriovenosas pulmonares (MAVP). Las MAVP fueron descritas a finales del siglo XIX y se correlacionan con la telangiectasia hemorrágica hereditaria. Generalmente involucran el flujo arterial pulmonar y drenaje venoso pulmonar. Pueden ser asintomáticas o causar disnea, hemoptisis u otros síntomas. El diagnóstico incluye estudios de imagen como