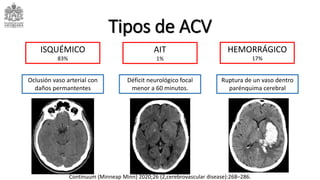
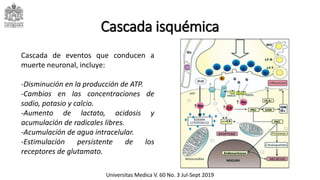
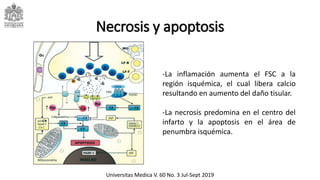
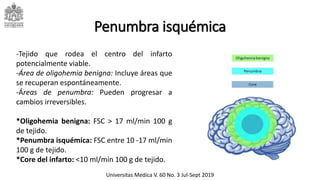
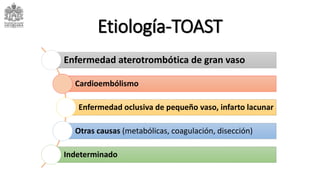
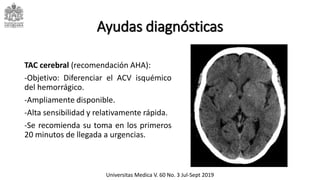
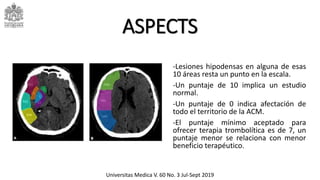
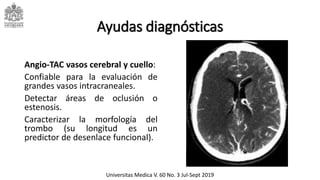
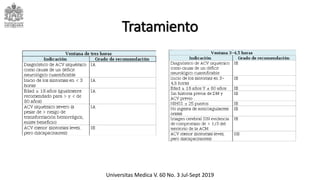
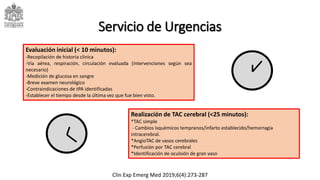
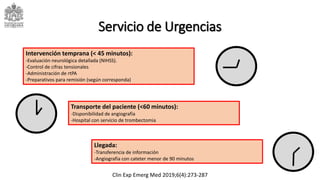
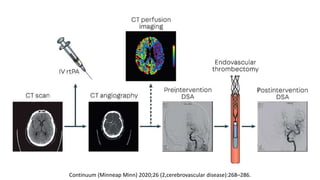
Este documento describe el ataque cerebrovascular (ACV), incluyendo su definición, tipos, epidemiología, fisiopatología, cuadro clínico, ayudas diagnósticas, tratamiento y manejo en el servicio de urgencias. El ACV es la segunda causa de muerte después de la enfermedad coronaria y causa discapacidad grave. El 83% de los ACV son isquémicos debido a oclusión vascular, mientras que el 17% son hemorrágicos. El tratamiento incluye trombólisis con alteplasa