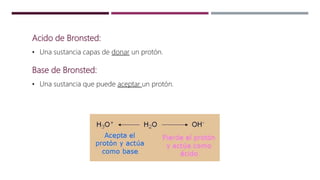
Un ácido de Bronsted es una sustancia que puede donar un protón, mientras que una base de Bronsted puede aceptar un protón. El agua puede actuar como ácido o base dependiendo de la sustancia con la que reaccione. El pH es una medida de la acidez o basicidad de una solución acuosa y se define como el logaritmo negativo de la concentración de iones hidrógeno.






![EL PRODUCTO IÓNICO DEL AGUA
El estudio de la concentración del ion hidrogeno es muy importante, ya que indica la
acidez o basicidad de una disolución.
Ya que solo una fracción muy pequeña de moléculas de agua se ioniza, la
concentración del agua [H2O]. Permanece virtualmente sin cambios.](https://image.slidesharecdn.com/acidosybasesdebronsted-171002012358/85/Acidos-y-bases-de-bronsted-8-320.jpg)





![15.3 EL PH: UNA MEDIDA DE ACIDEZ.
El pH de una disolución se define como el logaritmo negativo de la concentración del
ion hidrógeno (en mol/L).
El logaritmo negativo proporciona un numero positivo para el pH, el cual, de otra
manera, seria negativo debido al pequeño valor de [H+ ].
El pH de una disolución es una cantidad adimensional.](https://image.slidesharecdn.com/acidosybasesdebronsted-171002012358/85/Acidos-y-bases-de-bronsted-14-320.jpg)








![EJERCICIOS DE PRACTICA:
1. El pH de lluvia recolectada en determinada región del noroeste de Estados Unidos en un
día en particular fue de 4.82. Calcule la concentración del ion H+ del agua de lluvia.
2. En una disolución de NaOH [OH-] es de 2.9x10-4 M. Calcule el pH de la disolución.
3. El acido nítrico (HNO3) se utiliza en la producción de fertilizantes, colorantes,
medicamentos y explosivos. Calcule el pH de una disolución de HNO3 que tiene una
concentración de ion hidrógeno de 0.76 M.](https://image.slidesharecdn.com/acidosybasesdebronsted-171002012358/85/Acidos-y-bases-de-bronsted-23-320.jpg)