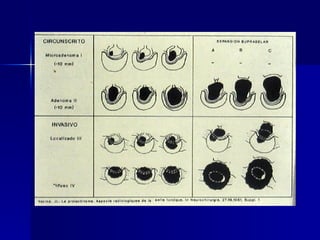
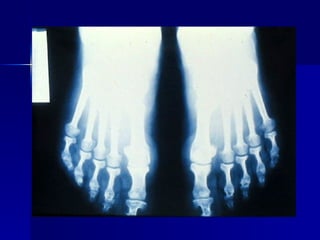
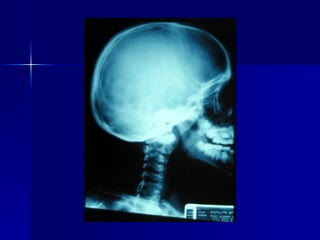
El documento habla sobre tumores hipofisiarios. Menciona que pueden ser adenomas o carcinomas, y clasificarlos por tamaño, función y morfología. Explica que los tumores hipofisiarios más comunes son los prolactinomas y los productores de hGH. Describe los síntomas y formas de diagnosticar y tratar diferentes tipos de tumores hipofisiarios, incluyendo los prolactinomas y los tumores que causan hipersecreción de hGH.