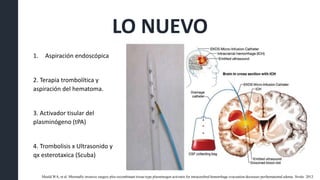
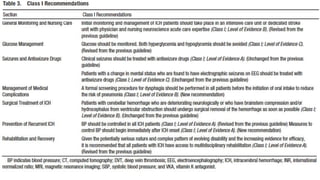
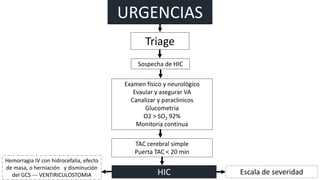
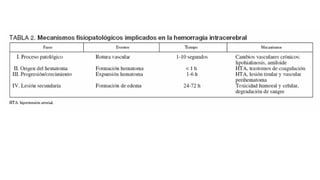
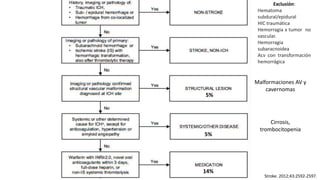
Este documento resume la hemorragia intracerebral (HIC), una emergencia médica grave. La HIC ocurre cuando se forma un coágulo de sangre en el cerebro, generalmente debido a la hipertensión arterial no controlada. Puede causar deterioro neurológico rápido y tiene una alta tasa de mortalidad y morbilidad. Se requiere identificación temprana mediante tomografía computarizada o resonancia magnética para guiar el tratamiento urgente, que puede incluir cirugía. La expansión del hematoma inicial predice un peor



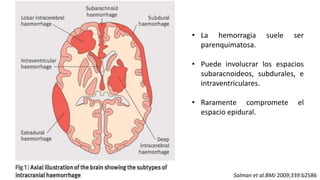








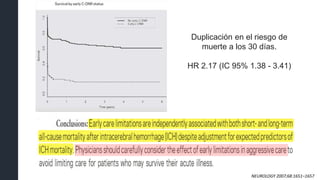
![Diringer MN, Edwards DF. Admission to a neurologic/neurosurgical intensive care unit is associated with reduced mortality rate after
intracerebral hemorrhage. Crit Care Med. 2001.
Survival function of the Cox survival analysis plotted as the mean of the covariates
identified in the multiple regression indicating cumulative survival of patients admitted to
neurologic/ neurosurgical (Neuro) and general intensive care units.
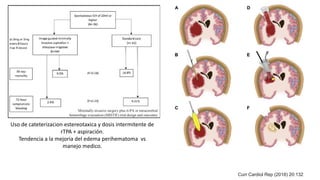
[OR], 3.4; 95% [CI], 1.65–7.6
Mejores
cuidados menor
mortalidad](https://image.slidesharecdn.com/hic-190719064258/85/Hemorragia-intracerebral-18-320.jpg)

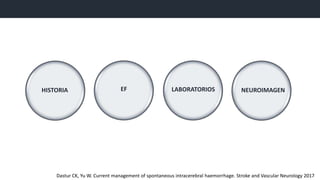































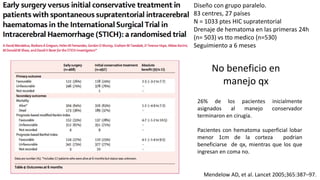
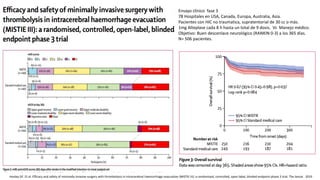
![Pacientes conscientes con HIC lobar superficial de 10 –
100ml sin hemorragia intraventricular 48h del ingreso.
78 centros, 27 países. N= 601 ptes
Qx temprana (12h) (307)vs manejo medico. (294)
Descenlace: pronóstico favorable o desfavolarble con
Glasgow extendido.
Resultados no favorables
59% qx. Vs 62 % médico.
Diferencia absoluta 3·7% [95% CI –4·3
- 11·6], OT 0·86 [0·62 - 1·20]; p=0·367
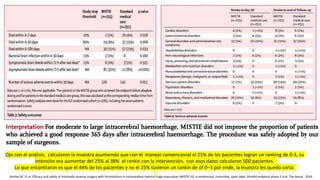
La cirugía temprana no aumenta la tasa de muerte o
discapacidad en 6 meses y podría tener una ventaja de
supervivencia pequeña pero clínicamente relevante para
los pacientes con HIC sin hemorragia intraventricular.
Lancet 2013;382:397–](https://image.slidesharecdn.com/hic-190719064258/85/Hemorragia-intracerebral-91-320.jpg)