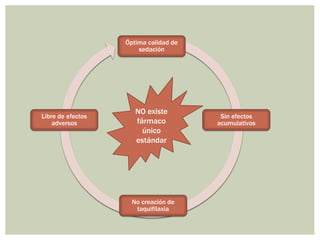
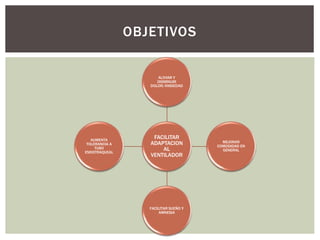
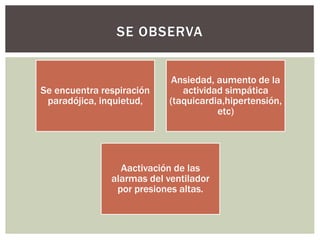
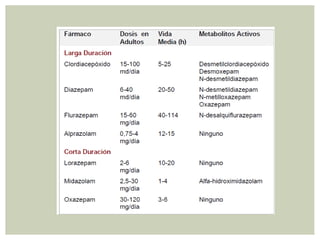
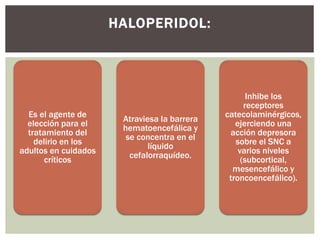
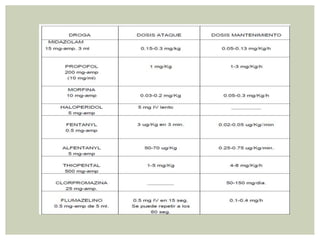
El documento discute la sedación en pacientes con ventilación mecánica. Explica que la sedación debe facilitar la adaptación al ventilador y aliviar el dolor y la ansiedad de forma segura. Detalla los objetivos, complicaciones potenciales y opciones de fármacos como benzodiacepinas, propofol, opioides y haloperidol para lograr una sedación óptima.